

- 2022-07-04 17:00:00
- 4033
2022年7月4日,武漢友芝友生物制藥股份有限公司(以下簡稱“友芝友生物”)自主研發(fā)的“注射用重組抗EpCAM和CD3 雙特異性抗體”(代號:M701),獲得國家藥品監(jiān)督管理局(NMPA)臨床試驗默示許可(受理號:CXSL2200178),公司將依據臨床批件的要求,近期在浙江省腫瘤醫(yī)院等多家中心開展M701治療惡性胸水的Ib/II期臨床研究。

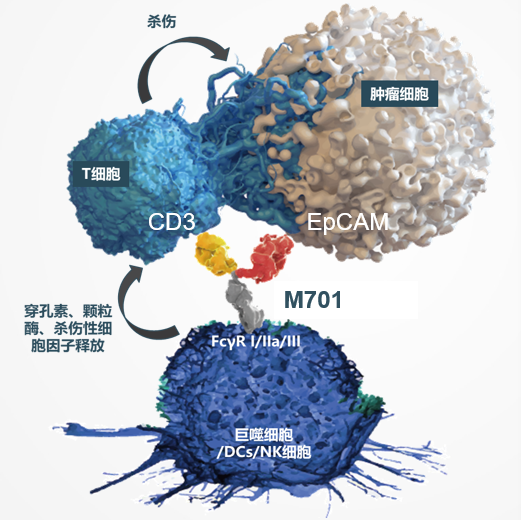
M701是友芝友生物通過自主專利非對稱雙特異性抗體YBODY®平臺開發(fā)的同時靶向EpCAM和CD3的生物一類新藥,已于2016年獲批開展治療惡性腹水的臨床研究,是中國第2個由國內企業(yè)研制并獲批進入臨床的雙特異性抗體。EpCAM(上皮細胞粘附分子)是上皮惡性腫瘤細胞表面最常見的特異性抗原,M701雙抗一端靶向EpCAM抗原,同時通過另一端CD3抗體可以橋接T細胞并激活T細胞殺傷EpCAM陽性腫瘤細胞。惡性腹水是我國高發(fā)的消化系統腫瘤和女性生殖系統腫瘤患者的晚期表現,嚴重影響患者的生存質量,缺乏理想的治療藥物。M701治療惡性腹水的I期臨床中期結果已于2021年9月在ESMO年會上發(fā)表,展現了良好的安全性和腹水控制效果。目前,M701正在開展聯合全身治療對惡性腹水的II期安全性和療效研究,與腹腔化療組相比已初步顯示出更好的腹水控制效果。
中國有大量癌癥患者會并發(fā)惡性胸水,僅肺癌患者每年就有超過34.4萬人并發(fā)胸水。胸水導致腫瘤患者出現呼吸困難、胸痛等癥狀,嚴重降低患者的生活質量,還會縮短腫瘤患者接受全身治療的機會,間接降低患者的生存時間,因此臨床上急需治療惡性胸水的有效藥物。惡性胸水與惡性腹水具有類似的發(fā)病機制,M701在惡性腹水II期臨床研究的同時,拓展惡性胸水適應癥,具有人體安全性驗證的基礎和科學依據,更好地滿足未滿足的患者需求,提升相關腫瘤患者的生存質量和生存率,有望給惡性胸水患者提供一種新的安全有效的治療手段。






